
 Antoine Laurent de Lavoisier (1743 - 1794) :
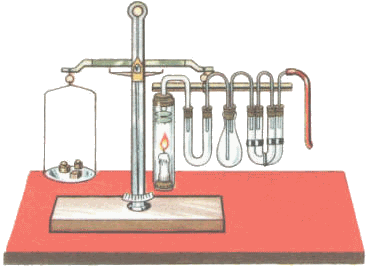
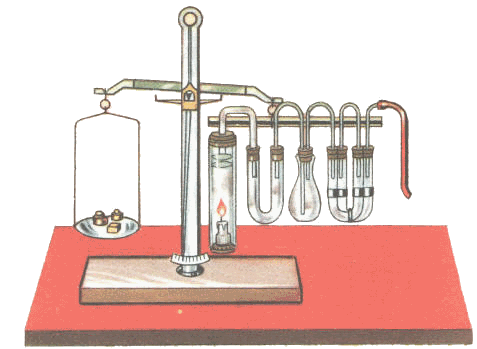
Antoine Laurent de Lavoisier (1743 - 1794) : Rien ne se perd, rien ne se crée, tout se transforme.reprenant la formule d'Anaxagore de Clazomènes (-500 - -428) :
Rien ne naît ni ne périt, mais des choses déjà existantes se combinent, puis se séparent de nouveau.
| C6H5C | + 7 O2 | → | 6 CO2 | + 2 H2O | + HC | ||
| charge | 0 | + 7 × 0 | = 0 | 6 × 0 | + 2 × 0 | + 0 | = 0 |
| C | 6 | + 7 × 0 | = 6 | 6 × 1 | + 2 × 0 | + 0 | = 6 |
| O | 0 | + 7 × 2 | = 14 | 6 × 2 | + 2 × 1 | + 0 | = 14 |
| H | 5 | + 7 × 0 | = 5 | 6 × 0 | + 2 × 2 | + 1 | = 5 |
| C | 1 | + 7 × 0 | = 1 | 6 × 0 | + 2 × 0 | + 1 | = 1 |
| NaHCO3 | + CH3CH2OH | → | CO2 | + Na+ | + CH3CH2O- | + H2O | ||
| charge | 0 | + 0 | = 0 | 0 | + 1 | + -1 | + 0 | = 0 |
| C | 1 | + 2 | = 3 | 1 | + 0 | + 2 | + 0 | = 3 |
| O | 3 | + 1 | = 4 | 2 | + 0 | + 1 | + 1 | = 4 |
| Na | 1 | + 0 | = 1 | 0 | + 1 | + 0 | + 0 | = 1 |
| H | 1 | + 6 | = 7 | 0 | + 0 | + 5 | + 2 | = 7 |